Pollution et accidents industriels – par exemple Lubrizol en septembre 2019, AZF en 2001, ou encore à Bhopal, en Inde, en 1984 – contribuent largement à ternir l’image de la chimie auprès du grand public. En parallèle, une prise de conscience de la nécessité à protéger l’environnement est née au cours de la deuxième moitié du 20ème siècle. L’évolution des mentalités pousse les chercheurs à repenser la chimie afin de l’adapter aux problématiques de son temps.
L’industrie chimique dite “de chimie lourde” transforme des matières premières, comme des minéraux ou des résidus de l’exploitation pétrolière, pour en faire différents produits, souvent à haute valeur ajoutée, qui seront utilisés par d’autres industries ou par le consommateur final : chlore, soude, matières plastiques ou caoutchoucs synthétiques, etc. Par opposition, la chimie “fine” est une autre branche de l’industrie chimique visant à synthétiser les principes actifs utilisés en cosmétique et pharmaceutique. De manière générale, l’industrie chimique est tenue par la loi de retraiter ses déchets, et notamment par le Code de l’Environnement depuis 1975. À titre d’exemple, la France produit en moyenne 1,2 millions de tonnes de déchets chimiques dangereux par an (chiffres 2014 et 2016).
Verdir la chimie à la source
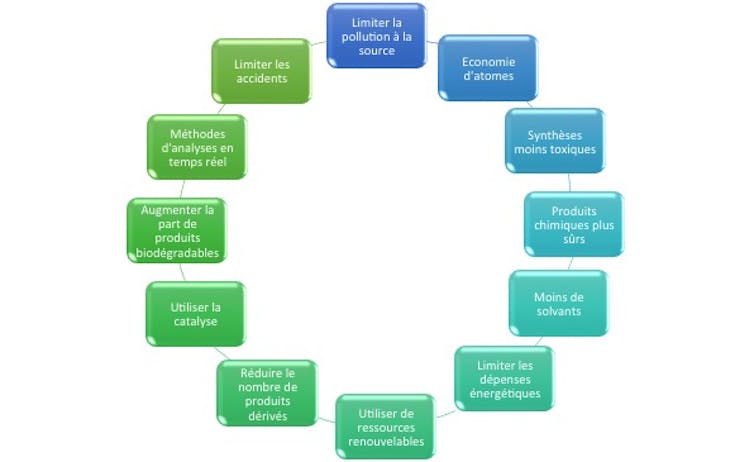
Le concept de chimie verte est né dans les années 1990 avec pour but de réduire l’impact néfaste du génie chimique sur l’environnement en traitant le problème à sa source. Il ne s’agit plus de chercher à retraiter les déchets pour limiter leur impact, mais bien de réduire au maximum la production de déchets au cours des différentes réactions menant au produit désiré. Pour ce faire, les réactions chimiques sont petit à petit retravaillées en prenant en compte les douze principes fondateurs fondateurs décrits par les chimistes P. Anastas et J. Warner.
Ces préceptes encouragent à réduire la production de déchets, à limiter la quantité d’énergie nécessaire pour réaliser les réactions, à utiliser des catalyseurs (molécules ajoutées aux mélanges qui permettent d’accélérer considérablement les réactions chimiques et sont réutilisables presque indéfiniment) et des matières premières renouvelables, à supprimer au maximum les étapes de synthèse superflues et à économiser les atomes : les réactifs doivent être choisis de manière à ce que le maximum de leurs atomes soient retrouvés dans le produit de réaction.
Pour atteindre ces buts, de nouvelles méthodes et outils sont développés. Certaines synthèses nécessitant des quantités parfois astronomiques de solvants peuvent être optimisées en utilisant par exemple des procédés mécaniques (broyage, agitation longue…) ou des fluides supercritiques (état de la matière obtenu à haute température et forte pression, donnant des propriétés intermédiaires entre celle des liquides et des gaz).
La chimie verte gagne petit à petit en importance : en 2001 et 2005, les prix Nobel de chimie ont été attribués à K.B. Sharpless et Y. Chauvin, qui ont conçu des réactions répondant à un ou plusieurs principes de la chimie verte. En parallèle, la réglementation évolue et impose maintenant des quotas aux industries : pour le secteur des carburants par exemple, la part de matières premières renouvelables imposée est passée de 5,3 % à 15 % entre 2005 et 2015.
Une application frappante de la chimie verte est la synthèse de l’ibuprofène (nom commercial d’un anti-inflammatoire). Le procédé classique génère 20000 tonnes de déchets, des sous-produits inutilisables, pour 13000 tonnes de médicament synthétisé en un an. Le procédé « chimie verte » produit un seul sous-produit, l’acide acétique, qui est revalorisable (comme solvant, coagulant, additif dans l’industrie alimentaire ou du tabac, etc.) et n’est donc pas un déchet. De plus, la nouvelle synthèse ne nécessite que 3 étapes, soit deux fois moins que l’ancienne réaction, ce qui se traduit par un gain important de temps et d’argent.
La biologie à la rescousse
Il existe de nombreuses façons d’aborder la chimie verte. La bio-ingénierie utilise des cellules et bactéries pour réaliser des réactions chimiques qui sont complexes et coûteuses en laboratoire. En effet, la nature nous offre un savoir-faire jusque là inégalé par la technologie, et l’utilisation d’organismes vivants élargit considérablement le champ des possibles. Les cellules et les enzymes par exemple réalisent de nombreuses réactions chimiques plus vite et plus efficacement que nous.
Leur étude et leur compréhension a conduit au développement de deux approches différentes. D’une part, la nature est devenue une nouvelle source d’inspiration majeure pour les chercheurs. De son observation et de la compréhension fine des mécanismes est née le biomimétisme. Les scientifiques se sont inspirés des capacités des geckos à s’accrocher aux surfaces pour développer de nouveaux adhésifs, de la résistance des toiles d’araignée pour améliorer les gilets pare-balles, de l’hydrophobicité du lotus pour inventer de nouveaux revêtements de salle de bain, de l’architecture des termitières pour inventer des logements plus écologiques.
Certains chercheurs cherchent aussi à « apprivoiser » bactéries et levures afin d’exploiter leur savoir-faire. Le cas le plus parlant aujourd’hui est probablement celui d’Ideonella sakaiensis, une bactérie dévoreuse de plastique découverte par hasard en 2016. Cette bactérie produit une enzyme pouvant dégrader le PET, polymère constitutif de nos bouteilles en plastiques. Dans le contexte actuel, où 1 million de bouteilles en plastiques sont vendues par minute dans le monde et 1,6 million de kilomètres carrés (soit 3 fois la surface de la France) de plastiques flotte actuellement dans l’océan Pacifique, ce type de découverte peut devenir une avancée majeure pour l’écologie et la santé. Cependant, cette biotechnologie reste confinée au laboratoire en attendant d’être mieux développée, car elle s’applique seulement à certains types de plastiques – l’enjeu serait d’élargir son champ d’action.
Des cristaux de protéines pour guider les réactions chimiques
D’autres outils, encore méconnus aujourd’hui, se révèlent pourtant très prometteurs. C’est le cas notamment des cristaux de protéines. Les cristaux les plus communs sont le sel, la neige, des pierres précieuses… ils présentent tous la particularité de répéter des motifs de façon régulière. Et bien que les protéines soient de gros objets, chimiquement parlant, on peut aussi les faire cristalliser.

La cristallisation de protéines a d’abord représenté une avancée majeure pour la médecine. En effet, les protéines sont de grosses molécules dont les structures, complexes et difficiles à étudier, sont intimement liées à leurs fonctions chimiques et biologiques. La meilleure façon d’étudier leur structure 3D est l’irradiation par rayons X mais l’utilisation de cette technique n’est pas envisageable sur une protéine isolée, car elle serait dégradée ; un cristal de protéine contient 1015 molécules ayant la même orientation et est plus résistant à l’irradiation. Étudier un cristal donne accès à la structure 3D d’une protéine, ce qui permet de comprendre ses interactions avec son environnement et d’étudier comment fonctionne son site actif (lieu de la protéine dans lequel sont réalisées les transformations chimiques). Il est donc beaucoup plus facile de prédire avec quel type de médicament elle sera capable d’interagir.
En ce qui concerne la chimie verte, ce sont les propriétés chimiques des cristaux de protéines qui sont exploitées. En effet, en obtenant des arrangements spécifiques des cristaux de protéines, on peut exposer des éléments chimiques particuliers parmi les acides aminés constituant les protéines (petites molécules constituées d’atomes de carbone, d’oxygène, d’azote et de soufre) et ainsi favoriser certaines réactions. Par exemple, dans certains cas très particuliers, le cristal s’arrange sous forme de réseau tridimensionnel semblable à un nid d’abeille. Des réactions chimiques peuvent être envisagées dans les alvéoles, car la paroi des tubes est constituée d’acides aminés qui peuvent interagir avec leur environnement et où un certain nombre de molécules peuvent se greffer.
Ce type de cristaux de protéines a fait l’objet d’un brevet récent et est à l’étude, car il pourrait permettre de manipuler de très petits objets de taille nanométrique et de rapprocher les partenaires d’une réaction chimique, diminuant ainsi les temps de réaction. De plus, en greffant de petites molécules utiles chimiquement sur les acides aminés de la paroi des tubes afin de favoriser les réactions désirées, ces cristaux de protéines pourraient devenir de puissants catalyseurs pour diverses réactions. Enfin, l’environnement des tubes, comme la lumière, l’air ou l’eau, pourrait servir de sources d’énergie ou de matière, permettant d’appliquer différents principes de la chimie verte.

