Alors que nous fêtons le 70e anniversaire de la découverte de la structure de l'ADN, les vaccins à acide nucléique (ADN et ARN) sont aujourd'hui d'une importance cruciale, notamment depuis la pandémie de Covid-19.
En quoi consistent ces vaccins, et comment fonctionnent-ils ?
Les vaccins à acides nucléiques, une nouvelle approche vaccinale
Pour comprendre en quoi les vaccins à acides nucléiques diffèrent des vaccins classiques, il faut revenir sur le principe de la vaccination préventive.
Cette approche consiste à injecter dans l’organisme de faibles doses d’un agent pathogène (virus ou bactérie) ou des fragments d’agent pathogène, pour exposer le système immunitaire et le préparer à contrer les attaques futures.
Tous les vaccins actuels reposent sur ce principe, qu’il s’agisse de vaccins atténués (contenant un agent pathogène vivant dont la virulence a été a amoindrie), de vaccins inactivés (à base d’agents pathogènes entiers tués), de vaccins « sous-unitaires » (basés sur l’emploi de fragments d’agents pathogènes purifiés) ou de vaccins issus du génie génétique (le fragment d’agent infectieux utilisé est produit par des cellules cultivées en laboratoire, et non plus à partir de microbes purifiés).
Read more: Vaccins vivants atténués : pourquoi il ne faut pas renoncer à les utiliser
Dans le cas des vaccins à ADN et ARN, le principe est fondamentalement différent : il s’agit de faire produire les fragments d’agents infectieux capables de stimuler la réponse immunitaire directement par les cellules du patient.
Comment fonctionnent les vaccins à acides nucléiques ?
Si l’ADN, support de l’information génétique, est une molécule qui est aujourd’hui plutôt familière, l’ARN est moins connue.
Chimiquement proche de l’ADN, mais moins stable, L’ARN joue divers rôles dans nos cellules, mais c’est en particulier un intermédiaire indispensable à la production de protéines.
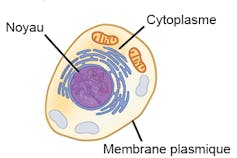
Schématiquement : la fabrication d’une protéine débute dans le noyau de la cellule, où se trouve l’ADN. Dans un premier temps, la portion de la molécule d’ADN correspondant à la protéine à produire est copiée sous forme d’ARN. Cette molécule d’ARN quitte ensuite le noyau : elle passe dans le cytoplasme de la cellule, où elle sera utilisée comme un « guide de montage » de la protéine.
Dans le cas des vaccins à ADN ou à ARN, l’idée est d’injecter au patient des molécules d’ADN ou d’ARN correspondant à des protéines de l’agent pathogène contre lequel on souhaite l’immuniser. Ces protéines sont choisies en fonction de leur capacité à provoquer une réponse immunitaire, ou « immunogénicité ». Après injection de l’ADN (ou l’ARN) correspondant, les cellules de l’individu à vacciner fabriqueront elles-mêmes lesdites protéines.
Le vaccin de Pfizer et BioNtech emploie un ARN messager codant pour la protéine Spike du coronavirus SARS-CoV-2 (prefusion spike glycoprotein - P2 S), la « clé » qui lui sert à entrer dans les cellules qu’il infecte.
Les avantages des vaccins à base d’ADN ou d’ARN
Plus faciles à fabriquer, grâce à une méthode de production standardisée, peu coûteuse, extrêmement bien définis d’un point de vue moléculaire, les vaccins à ADN et ARN ont un potentiel de développement très important et pourraient protéger à la fois contre des maladies infectieuses (vaccins prophylactiques) ou lutter contre des pathologies cancéreuses (vaccins thérapeutiques).
Ils sont aussi mieux maîtrisés que les vaccins « traditionnels », car ils n’utilisent pas de virus entiers comme dans les vaccins issus de virus vivants atténués, inactivés ou recombinants, ni d’adjuvants, mais simplement une molécule d’acides nucléiques (ADN ou ARN).
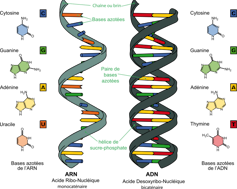
Les vaccins contenant de l’ADN sous forme de double hélice (une hélice constituée de deux brins) peuvent être stables à température ambiante (cette molécule est si résistante qu’elle permet de dater des objets très anciens tels que des momies), et ne nécessitent donc pas de respecter une quelconque chaîne du froid.
Il n’en va pas de même pour les vaccins basés sur des ARN messagers : leur structure, constituée d’un seul brin, est sensible aux enzymes qui découpent l’ARN (appelées « RNAses »). C’est la raison pour laquelle ces vaccins sont conservés à -70°C, pour éviter toute dégradation enzymatique.
Le vaccin de Pfizer et BioNtech entrant dans cette catégorie, certains observateurs ont souligné le défi logistique que représentera sa distribution.
Comment arriver à bon port ?
Cette nouvelle méthode de vaccination sera beaucoup plus réactive pour produire des vaccins extrêmement rapidement, ce qui permettra de répondre à des menaces d’infections liés à des nouveaux agents infectieux, ou de proposer de nouvelles méthodes de traitement du cancer. Ces avantages expliquent l’essor des recherches sur ce nouveau type de vaccination ces trente dernières années, et permet d’envisager les vaccins ADN et ARN comme les « vaccins du futur ».
Des difficultés subsistent néanmoins pour assurer complètement l’efficacité des vaccins à acides nucléiques. L’un des obstacles principaux consiste à réussir à amener les molécules d’ADN ou d’ARN au bon endroit de la cellule : dans le noyau pour les premières, et dans le cytoplasme pour les secondes. Il faut pour cela franchir les membranes des cellules, dont l’un des rôles est précisément de servir de barrière aux envahisseurs, et éviter la dégradation par les enzymes cellulaires.
Pour y parvenir, plusieurs solutions sont possibles. On peut utiliser un virus modifié pour servir de « moyen de transport » à l’acide nucléique que l’on souhaite introduire dans les cellules. Une autre approche consiste à fabriquer de toutes pièces une enveloppe artificielle, une sorte de virus synthétique. C’est cette piste qu’ont choisie Pfizer et BioNtech, qui ont utilisé des particules nanolipidiques pour transporter l’ARN vaccinal.
Notre équipe a quant à elle mis au point des véhicules un peu particuliers, appelés Nanotaxi®. À base de polymères en forme d’étoile ou de lipides dérivés de sucres naturels, ils peuvent soit franchir directement la membrane en transportant avec eux les ADN ou ARN destinés à la vaccination, soit entrer dans la cellule par les voies employées naturellement par les substances « autorisées » à y pénétrer.
Ces deux modes d’entrée dans la cellule vont jouer un rôle décisif pour l’activation du système immunitaire. Ils vont en effet mettre en alerte le système de surveillance de la cellule, déclenchant la fabrication de molécules impliquées dans la réponse immunitaire. Celles-ci vont contribuer à l’augmentation de l’immunogénicité, et donc à l’efficacité du vaccin à ADN ou ARN.
Vers de nouveaux vaccins utilisés en santé humaine ?
Les vaccins à acides nucléiques ont déjà fait l’objet de nombreuses études précliniques et cliniques contre des cibles variées, dans le domaine des maladies infectieuses et de l’oncologie. Tous ces essais ont démontré la parfaite tolérance de ce type de vaccins.
Avant la survenue de la pandémie de Covid-19, quatre vaccins à ADN avaient déjà reçu les autorisations réglementaires nécessaires à leur exploitation chez l’animal. Il sont utilisés par exemple pour protéger les saumons d’élevage contre la nécrose hématopoïétique infectieuse et contre une maladie du pancréas, les poulets contre la grippe aviaire, ou pour soigner les chiens atteints d’un mélanome buccal.
Mais ces résultats prometteurs obtenus chez l’animal n’avaient pas encore été reproduits chez l’être humain : l’immunogénicité de ces vaccins restait insuffisante pour conférer aux patients une protection contre les agents pathogènes ciblés. L’autorisation de mise sur le marché semblait encore lointaine.
Désormais, avec l'administration du vaccin Pfizer, les résultats à venir pourraient changer la donne, et accélérer les recherches sur les vaccins à acides nucléiques. L’avenir (proche) nous le dira.