Cette année, le Téléthon se tiendra les 8 et 9 décembre. Cet évènement consacré aux maladies rares est l’occasion de lever le voile sur la drépanocytose qui est la maladie génétique rare la plus fréquente en France, avec environ 30 000 personnes atteintes.
Cette pathologie reste pourtant insuffisamment connue de certains professionnels de santé et, plus généralement, de la société. La drépanocytose est également très répandue dans le monde, notamment en Afrique, dans les Antilles et au Moyen-Orient.
Anémie, crises douloureuses et impact majeur sur la qualité de vie
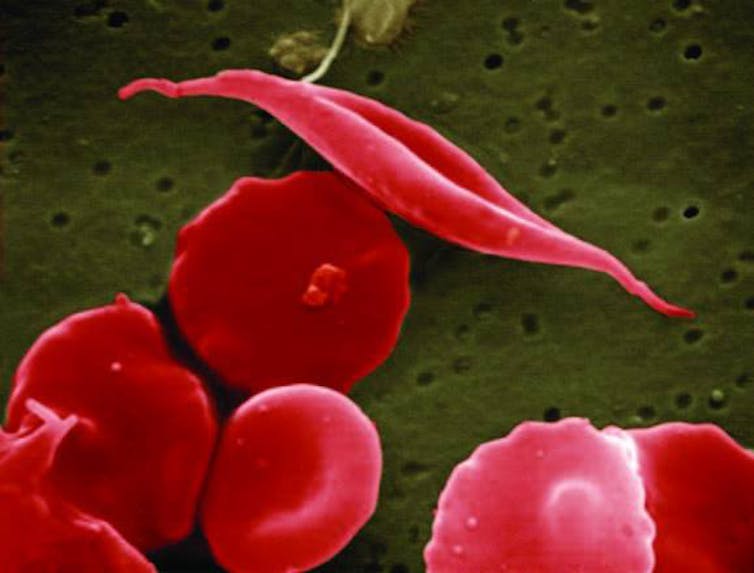
La drépanocytose est due à une anomalie de l’hémoglobine, principal composant des globules rouges, qui sont des cellules du sang permettant le transport de l’oxygène aux organes.
Cette anomalie cause une déformation des globules rouges qui prennent une forme de faucille (d’où son autre nom d’anémie falciforme). Cela entraîne leur destruction (anémie) et des occlusions des petits vaisseaux sanguins responsables de crises très douloureuses appelées « crises vaso-occlusives ».
De plus, la drépanocytose peut atteindre les vaisseaux de tous les organes conduisant à des lésions graves et multiples (atteintes des artères cérébrales, atteintes pulmonaires, cardiaques, rénales, hépatiques, etc.). Cette maladie est responsable de décès précoces et a un impact majeur sur la qualité de vie des patients qui est à ce jour mal évalué.
Se construire entre les crises
Alors que, dans d’autres maladies génétiques, les symptômes peuvent s’exprimer de manière continue, les personnes atteintes de drépanocytose se construisent dans l’alternance entre des périodes de « vie normale » et des épisodes de crises, dont ils qualifient la douleur d’« insoutenable », « invivable », « traumatique ».
En crise ils se sentent malades, le reste du temps ils se savent malades, anxieux de l’advenue de ces crises menaçantes et soumis aux contraintes à respecter pour les éviter (s’hydrater, ne pas s’exposer au froid, aux émotions fortes, ne pas faire trop de sport, etc.).
La drépanocytose peut ainsi être qualifiée de « maladie chronique de l’aigu » du fait des ruptures répétées et imprévisibles que ces crises occasionnent. Celles-ci paralysent physiquement, mais hypothèquent aussi tout projet de vie, même minime ou à court terme. De plus, le fait que ce soit une maladie mortelle engage les patients dans une lutte pour la survie.
Finalement, ces crises impactent le sentiment de continuité de l’existence ou la continuité de la conscience (la perception d’être le même dans l’espace et dans le temps), socle de l’identité personnelle. Pour faire face psychologiquement aux douleurs extrêmes qu’elles génèrent, de nombreux patients mettent en place des mécanismes qui consistent à se déconnecter de leurs corps et de leurs émotions.
La greffe de moelle, seul traitement curatif
Les principaux traitements (médicaments par voie orale et échanges transfusionnels consistant à retirer du sang du patient et à le transfuser avec des globules rouges sains) permettent d’atténuer la maladie, sans toutefois la faire disparaître. De plus, chez certains patients, ces traitements sont inefficaces.
À l’heure actuelle, le seul traitement curatif est la greffe de moelle osseuse. Présente à l’intérieur des os, celle-ci fabrique toutes les cellules du sang. La greffe permet de remplacer la moelle du patient qui fabrique des globules rouges malades, par celle d’un donneur qui fabrique des globules rouges sains.
Ce traitement permet d’améliorer les symptômes et de guérir la maladie de la majorité des patients. Cependant la greffe peut être responsable de complications qui sont plus fréquentes lorsqu’elle est réalisée chez les adultes. Ainsi, 75 % des greffes de moelle (sur environ 700) pratiquées à ce jour en France chez des patients atteints de drépanocytose, l’ont été chez des enfants de moins de 15 ans, selon la Société francophone de greffe de moelle et de thérapie cellulaire.
Effets psychosociaux inattendus de la « guérison »
L’évolution des techniques de greffe permet aujourd’hui de greffer des patients adultes avec une moindre toxicité et d’envisager des greffes chez des patients n’ayant pas de donneur parfaitement compatible. Ainsi, des patients adultes, ayant vécu des années avec cette maladie très lourde et considérée comme incurable, se retrouvent « guéris ».
Il a été constaté que cette guérison somatique (c’est-à-dire avec une diminution voire une disparition des symptômes) s’accompagnait chez certains patients d’effets inattendus sur le plan psychosocial et de difficultés à se réapproprier leur vie.
[Plus de 85 000 lecteurs font confiance aux newsletters de The Conversation pour mieux comprendre les grands enjeux du monde. Abonnez-vous aujourd’hui]
Cet apparent paradoxe, entre la promesse de guérison offerte par la médecine et certains vécus relatés par les patients, est un des objets de l’étude « Revivre » initiée par des chercheurs en sciences humaines et sociales et des équipes médicales, à partir des récits de vie de malades.
La greffe de moelle osseuse est ainsi l’occasion de penser ce que signifie vivre ou revivre après avoir fait l’expérience d’une maladie génétique dont les symptômes altèrent lourdement l’espérance et la qualité de vie, parfois dès la naissance.
Revivre après la greffe
La greffe de moelle osseuse n’est proposée, le plus souvent, qu’en dernier recours, après un épisode qui peut avoir fait frôler la mort. C’est un choix contraint, « quand on n’a plus rien à perdre » comme le disent certains patients. En dépit des informations données par les médecins et d’autres patients greffés, elle représente un « saut dans le vide ». Elle constitue à la fois une épreuve et une renaissance.
La vie après la greffe est décrite par les patients comme la possibilité de déployer et d’éprouver une « liberté de mouvement » ou une puissance d’agir toutes nouvelles. Revivre, c’est faire ce dont ils étaient incapables, s’autoriser à ressentir des émotions et faire des projets jusqu’ici interdits, gagner en confiance en soi, se sentir « comme les autres ».
Cependant, ces possibilités sont déstabilisantes parce que totalement inédites et survenant dans une temporalité accélérée qui ne permet pas de les intégrer psychologiquement ou émotionnellement. Elles bousculent les défenses psychiques mises en place pour faire face à la maladie, provoquant parfois des états de sidération. S’ouvre une temporalité nouvelle : un avenir définitivement libéré de l’imprévisibilité des crises, mais dans lequel il n’est pas évident de se projeter.
Un état de déséquilibre au moins transitoire
La greffe conduit ainsi à un état de déséquilibre au moins transitoire. Elle n’efface pas le passé ni les expériences corporelles, relationnelles, sociales liées à la maladie. Du fait des séquelles physiques, de la prise de médicaments et du suivi médical, la maladie demeure sous d’autres formes (stérilité, ostéonécrose – qui correspond à la destruction progressive de certains os, l’une des complications de la maladie –, addiction aux antidouleurs, etc.). Parfois, des douleurs (appelées « douleurs fantômes ») ressurgissent, faisant craindre aux patients un retour de la maladie et manifestant une anxiété toujours active.
Certains patients s’aperçoivent qu’ils ne peuvent pas faire « comme tout le monde », l’entrée dans la vie active en particulier s’avère complexe en raison de « tout ce qu’on n’a pas pu faire à cause de la maladie » (études, expériences professionnelles…).
Read more: Et si Gaston Lagaffe avait en réalité un syndrome d’Ehlers-Danlos ?
Enfin, la maladie reste transmissible, complexifiant la vie amoureuse et les projets parentaux. En effet, la drépanocytose est une maladie génétique héréditaire. Même traitée par greffe, une personne qui porte les gènes mutés responsables de la drépanocytose les transmet à son enfant.
L’après-greffe est le moment parfois douloureux de prendre la mesure de tout ce que la vie avec la drépanocytose a empêché et de tout ce qu’il semble difficile de rattraper dans une vie sans elle.
Être « autrement le même » : ni malade, ni en bonne santé
La question « Qui suis-je ? » émerge chez beaucoup de patients et montre une tension entre trois dimensions : une présence du passé qui est constitutif du soi, une « perte de soi » marquée par une sensation de vide, et le besoin de construire une « nouvelle identité ».
Les personnes se trouvent pour la plupart dans un entre-deux : ni malades – elles n’ont plus les symptômes de leur pathologie initiale –, ni en bonne santé – « ex-drépanocytaires » et pouvant toujours transmettre la maladie.
Certains préfèrent ne plus parler de la maladie, comme si l’oubli était « une réponse de la vie à ce qui en elle est invivable », nécessaire pour continuer ou recommencer à vivre. D’autres culpabilisent d’avoir été greffés.
L’apport des sciences humaines et sociales pour penser un soin global
Dans ce processus de transformation, il faut apprendre à se (re)connaître et se reconstruire, à devenir « autrement le même » ou « malade autrement », selon l’expression d’un patient greffé.
Être « autrement » évoque l’effort à déployer pour apprendre à vivre sans la maladie initiale mais avec d’autres vulnérabilités qui ne lui seront pas nécessairement liées ; être « le même » renvoie à la « nécessité vitale pour un individu d’avoir un sentiment de cohésion et de continuité quant à la perception de ce qu’il est ».
L’étude « Revivre » illustre l’apport indispensable des sciences humaines et sociales pour penser un soin global de la personne malade.
En éclairant les limites de la notion de guérison et la complexité du revivre, elle contribue, de manière utile aussi à d’autres maladies rares, à définir des filières, des réseaux et des pratiques (médicales et non médicales) de soin adaptés et susceptibles de soutenir l’empowerment ou la normativité des malades.
Cet article a été co-écrit par les trois auteures mentionnées et le Dr Nathalie Dhédin, médecin hématologue (Unité d’hématologie Adolescents et Jeunes Adultes, APHP- hôpital Saint-Louis) spécialisée dans la greffe de moelle osseuse en particulier des patients drépanocytaires, et à l’initiative du protocole de recherche mené en SHS sur cette thématique. Nous remercions tous les patients et soignants qui soutiennent et participent à cette étude.

Le projet IDEX est soutenu par l’Agence nationale de la recherche (ANR), qui finance en France la recherche sur projets. Elle a pour mission de soutenir et de promouvoir le développement de recherches fondamentales et finalisées dans toutes les disciplines, et de renforcer le dialogue entre science et société. Pour en savoir plus, consultez le site de l’ANR.