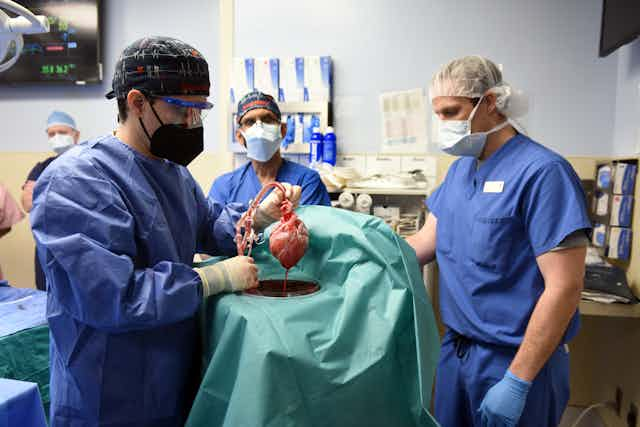
Le 10 janvier 2022, un communiqué de presse de l’École de médecine de l’Université du Maryland (États-Unis) annonçait qu’un patient avait été opéré trois jours plus tôt pour recevoir un cœur de cochon génétiquement modifié. Âgé de 57 ans et atteint d’une pathologie cardiaque en phase terminale, David Bennett Sr n’était pas éligible à une greffe classique. Il est devenu le premier être humain dont la vie pourrait avoir été sauvée grâce à une « xénotransplantation », autrement dit par la greffe d’un organe provenant d’un être vivant appartenant à une autre espèce. Professeur à l’Université de Paris et chef du service de chirurgie cardiaque à l’hôpital Bichat (AP-HP), Patrick Nataf revient sur les implications de cette prouesse technologique.
The Conversation : En tant que chirurgien cardiaque, que vous inspire cette transplantation ? S’agit-il effectivement d’une prouesse médicale ?
Patrick Nataf : En matière de geste chirurgical, une telle opération diffère peu de celles que l’on met en œuvre régulièrement chez l’être humain. Tout chirurgien cardiaque qui pratique la transplantation sait greffer un cœur dans une autre poitrine. Que celui-ci provienne d’un autre être humain ou d’un cochon voire d’un primate n’est pas l’essentiel. Tant qu’il existe une compatibilité anatomique et morphologique, on peut techniquement transplanter l’organe.
La véritable prouesse n’est pas tant chirurgicale qu’immunologique. Quand on greffe un organe d’une espèce sur une autre, il est généralement immédiatement rejeté par le corps du receveur (son système immunitaire le reconnaît comme étranger et le détruit). Le problème n’est donc pas tant de réussir chirurgicalement la transplantation que d’éviter ce rejet hyperaigu.
C’est l’exploit auquel sont parvenus les spécialistes qui se sont occupés de ce patient. Ils ont pour cela utilisé un cœur provenant d’une lignée de cochon génétiquement modifiée produite par la société américaine Revivicor.
TC : Sait-on quelles ont été les modifications apportées pour obtenir ce cœur de cochon « humanisé » ?
PN : En consultant les informations communiquées par l’Université du Maryland, on apprend que le génome de l’animal a été modifié de plusieurs façons. Trois gènes ont été inactivés : ils codaient pour des enzymes impliquées dans la fabrication de sucres présents à la surface des cellules cardiaques (et impliquées dans les mécanismes de rejet). Par ailleurs, six gènes humains ont été insérés, en vue d’améliorer l’acceptation du greffon par le corps du patient.
Enfin, un dernier gène porcin a été inactivé, afin d’éviter une croissance trop importante du cœur de l’animal. Il faut savoir que chez l’être humain, le capital de cellules cardiaques est fixé dans l’enfance et n’augmente que très peu tout au long de l’existence. Durant la croissance les cellules cardiaques ne se multiplient que très modérément. Elles grossissent, surtout, et ce faisant donnent au cœur sa forme.
Les manipulations effectuées sur les cochons de Revivicor semblent avoir permis d’éviter le rejet hyperaigu. Reste maintenant à observer comment vont évoluer les choses. Après une greffe, il peut en effet se produire différents types de rejets : le rejet hyperaigu, qui est immédiat, le rejet aigu, qui survient une à plusieurs semaines après la transplantation, et le rejet chronique, qui survient plus de 6 mois (et parfois des années) après l’opération.
Dans le cas présent, il est encore trop tôt pour avoir des certitudes quant à ce qui va se passer ensuite. Le rejet interespèce a-t-il été uniquement retardé ? Définitivement évité ? Cette dernière éventualité est relativement peu probable : les modifications génétiques n’ont évidemment pas permis d’éliminer tous les motifs moléculaires qui, sur ce greffon d’origine animale, pourraient être perçus par le système immunitaire du patient comme « étranger », et donc mener à son élimination.
Les thérapeutiques immunosuppressives (médicaments destinés à éviter le rejet, en limitant voire supprimant la réponse immunitaire du patient) associées habituellement à la greffe devront être évaluées et adaptées à ce type de transplantation.
TC : Pourquoi les scientifiques ont-ils choisi le cochon plutôt, par exemple, qu’une espèce de primate ?
PN : Premièrement, parce qu’anatomiquement, le cœur du cochon ressemble beaucoup au cœur de l’être humain. Greffer cet organe ne pose pas vraiment de problème, car sa configuration est approximativement la même que celle de notre cœur. Deuxième point important : les cochons s’élèvent plus facilement que les primates, et ils ont des portées nombreuses, régulières. Enfin, c’est un animal qui grandit assez vite.
On peut donc obtenir rapidement des cœurs de différentes tailles, de volumes variés, adaptés aux morphologies des personnes que l’on doit opérer. Il s’agit là d’un atout majeur du cochon par rapport à d’autres animaux.
TC : Pourrait-on imaginer de greffer d’autres organes que le cœur ? À la fin de l’année dernière, des chirurgiens américains avaient par exemple greffé avec succès un rein de cochon génétiquement modifié sur un patient en état de mort cérébrale…
PN : Anatomiquement, on peut chirurgicalement envisager la greffe d’à peu près tous les organes. Cependant il faut souligner qu’il existe des formes de rejet spécifiques à chaque organe et que chaque organe a des fonctions différentes. De ce point de vue, la complexité immunologique et fonctionnelle n’est pas la même selon l’organe considéré. Ce peut être une des limites pour généraliser à tous les organes ce type de transplantation.
TC : Au-delà des rejets, existe-t-il d’autres risques potentiels ?
PN : On ne peut pas éliminer complètement le risque d’une contamination par un agent pathogène. Même si ces cochons sont élevés dans des laboratoires où les conditions sont strictement contrôlées, et que les cœurs utilisés sont censés être indemnes de tout agent pathogène, on ne peut pas affirmer que le risque est nul.
On pourrait par exemple imaginer que, même si les zoonoses (maladies se transmettant de l’animal à l’humain) que l’on connaît sont bien contrôlées, certaines maladies jusqu’ici non encore identifiées puissent se révéler après transplantation. Un peu comme ce qui s’est passé durant la crise de la vache folle pour les maladies à prions… Il faut d’ailleurs se souvenir que c’est cette crise sanitaire qui a mis un violent coup de frein à la recherche sur les xénotransplantations, qui, en matière de recherche, avait le vent en poupe dans notre pays jusqu’au début des années 1990.
TC : Pourquoi cette technologie a-t-elle été choisie pour ce patient ? N’y avait-il pas d’autre solution ?
PN : Le patient qui a reçu cette xénogreffe était maintenu en vie grâce à une assistance respiratoire extra-corporelle (extracorporeal membrane oxygenation – ECMO). En d’autres termes, son sang était pompé au moyen de canules puis mis en circulation après son passage dans une machine destinée à l’oxygéner. Les ECMO ne pouvant être utilisées que pendant un laps de temps limité, ce type de patient est prioritaire pour obtenir un greffon. Mais il n’est pas toujours possible de lui en procurer un, du fait de l’incapacité de trouver un greffon humain compatible morphologiquement ou immunologiquement, ou encore en raison d’une dégradation de son état général, avec des défaillances pouvant toucher d’autres organes. Dans ces conditions, il faut envisager d’autres solutions.
Le chirurgien peut alors choisir d’installer un ventricule artificiel, comme solution temporaire ou à titre définitif. Il peut aussi envisager la pose d’un cœur artificiel total, tel celui mis au point par l’entreprise française Carmat, en attendant une transplantation. Mais ce type d’appareillage n’est pas disponible pour toutes les morphologies de patients, et il ne peut pas être utilisé systématiquement, cela dépend du type de défaillance observée. Par ailleurs, la pose de ces dispositifs n’est pas sans danger.
Outre les aléas liés à la chirurgie ou à la défaillance de la machine, il existe aussi des risques d’infection (les ventricules, par exemple, sont alimentés par des câbles qui sortent par la peau, et ces points peuvent s’infecter). Enfin, la qualité de vie des patients s’en ressent : ils doivent vivre en permanence avec une machine reliée soit à une prise de courant, soit à des batteries externes, ce qui limite leur autonomie.
Les xénogreffes pourraient constituer des organes de transition, voire de remplacement définitif. Si elles devenaient un jour largement disponibles, cela permettrait peut-être de limiter l’impact de la pénurie à laquelle nous faisons face, malgré une législation aujourd’hui très en faveur du prélèvement d’organe en cas de décès. Chaque année, en France, environ 800 patients attendent une greffe du cœur, mais seuls 400 sont transplantés, faute de greffons. Dans le cas des autres organes, environ 20 000 patients sont en attente d’une transplantation (de foie, poumons, rein, etc.). Seuls 5000 d’entre eux en recevront une, tandis que 1500 décéderont faute de greffon.
TC : Mais quand bien même cette première chirurgicale se solderait par un succès, il ne s’agit pour l’instant que d’un premier essai. Cette technologie n’est pas près d’être démocratisée…
PN : Non. Mais surtout, les enjeux ne se limitent pas aux questions de disponibilité ou de faisabilité technique. Selon moi, le défi posé par les xénogreffes n’est pas seulement chirurgical, immunologique, ou infectieux. Il est avant tout éthique, psychologique et sociétal, et nécessite de prendre le temps de la réflexion.
Quel sera le niveau d’acceptation des xénogreffes par la population, les instances politiques, religieuses, les ONG, etc. ? Certes, on implante déjà en routine des valves cardiaques de porc pour remplacer celles, défectueuses, de certains patients. Mais annoncer à quelqu’un qu’on va lui greffer un cœur d’animal complet, en remplacement du sien, n’a probablement pas les mêmes implications psychologiques. Cela pourrait poser problème à certaines personnes. Et à l’heure où certains s’inquiètent de l’exploitation et de la souffrance des animaux, que penser de cette approche qui les instrumentalise ? Sans même parler du fait que ces animaux sont des organismes génétiquement modifiés, nécessitant de recourir à des technologies qui polarisent fortement les débats, elles aussi. Prendre le temps de se pencher sur toutes ces questions, importantes, est essentiel. Rappelons qu’à ses débuts, la transplantation cardiaque entre humains elle-même a été très décriée…
Mais au-delà de ces questions se pose aussi la place de la recherche française dans le paysage international. Aujourd’hui, dans le secteur des xénogreffes, et plus largement de la recherche sur la transplantation, la France est distancée par les États-Unis, la Chine, l’Allemagne ou le Japon, alors même que nos équipes de transplantation sont très performantes. Notre recherche doit rester compétitive. Pour cela, des investissements majeurs sont à prévoir afin de parvenir à regrouper toutes les compétences de haut niveau sur ce thème.
Une solution serait de créer un institut hospitalo-universitaire (IHU) spécialisé dans la transplantation multiorganes (labellisés par l’État, les IHU sont des pôles d’excellence visant à fédérer recherche, soin, formation et transfert de technologies dans le domaine biomédical. Il en existe 6 en France actuellement, ndlr). Nous travaillons actuellement sur le Campus Nord Parisien à la réalisation de ce projet, qui réunirait les médecins, chirurgiens, chercheurs de tout type, spécialistes des questions de transplantations et d’innovation dans ce domaine.