Pour comprendre les processus pathologiques qui nous rendent malades, il faut pouvoir observer le très, très petit : être capable de distinguer l’architecture des cellules à l’échelle moléculaire permet de comprendre leur fonctionnement. La difficulté majeure : lorsque l’on observe des cellules de quelques microns (millionième de mètre) sous un microscope optique, nous n’arrivons pas à voir les molécules qui sont à l’intérieur car elles sont de taille nanométrique, un milliardième de mètre. Et nous n’avons pas accès à cette échelle.
Pourquoi ne peut on pas simplement faire comme dans les séries TV « scientifiques » américaines et zoomer à volonté les images jusqu’à voir les molécules ? Les propriétés de la lumière visible font que lorsque l’on tente d’observer une molécule nanométrique qui émet de la lumière, celle-ci produit une tâche sur la caméra de l’ordre du micromètre. Cette tâche résulte de la propagation de la lumière elle-même et ne peut donc être réduite. Zoomer revient alors à agrandir les taches et non à distinguer des détails plus fins. Pour les objets ayant une forte densité de molécules émettrices, ce qui est le cas des cellules, il est même impossible de distinguer les taches individuelles : celles-ci se superposent sur la caméra pour former l’image de l’objet.
Un phénomène analogue se produit lorsque l’on observe de loin une affiche de publicité ou un tableau pointilliste, les petits points du tramage ne peuvent être distingués. Chaque point produit sur la rétine une tache, les taches se chevauchent pour produire l’impression visuelle recherchée de l’ensemble du tableau. C’est pour cette raison qu’un microscope ne pourra jamais devenir un nanoscope… Du moins c’est ce que l’on croyait jusqu’à il y a environ 10 ans. Pour y parvenir, il aura fallu deux découvertes révolutionnaires qui ont chacune été récompensées par deux prix Nobels.
Lumière moléculaire
Tout d’abord, pour détecter les molécules biologiques comme les protéines, il faut qu’elles émettent de la lumière ce qui n’est pas le cas habituellement. Une idée simple est de leur attacher une petite molécule qui émette de la lumière. Certaines molécules dites fluorescentes possèdent justement cette propriété très particulière d’émettre une lumière de couleur différente de celle avec lesquelles elles sont éclairées. La fluorescence est particulièrement intéressante car en utilisant un filtre coloré on peut totalement masquer la lumière d’illumination et ne voir que la lumière de fluorescence sur un fond complètement noir. Aujourd’hui avec des caméras très sensibles, il est ainsi possible de voir une seule molécule en train de fluorescer.

Mais comment être sûr que cette « lumière moléculaire » est bien attachée à la molécule que l’on cherche à suivre dans la cellule ? Ce n’est pas simple et la découverte qui a permis de résoudre ce casse-tête a été récompensée par un prix Nobel en 2008. Certaines méduses sont naturellement fluorescentes. Quand on les éclaire dans le bleu, elles émettent du vert. Elles fabriquent en fait une petite molécule qui est fluorescente. Il s’agit d’une petite protéine que l’on a surnommé protéine fluorescente verte. Aujourd’hui il est possible de modifier génétiquement tous les êtres vivants très facilement et d’insérer les gènes qui codent pour cette molécule. Ainsi, lorsque l’on veut comprendre le fonctionnement d’une cellule et suivre une protéine particulière synthétisée par cette cellule pour en comprendre le rôle, on modifie génétiquement la cellule pour introduire les gènes de cette petite protéine fluorescente avec ceux de la protéine à suivre. Lorsque la cellule va fabriquer cette dernière, elle lui accrochera automatiquement la protéine fluorescente qui servira alors d’émetteur de lumière et que l’on pourra suivre.
Il est donc possible d’accrocher une petite lampe moléculaire pour suivre spécifiquement, dans une cellule, les molécules que l’on veut, mais il faut encore pouvoir distinguer chaque point plutôt que des taches entremêlées… Si l’on pouvait « allumer » un seul point du tableau, ou quelques points suffisamment espacés, alors il serait possible de bien distinguer chaque tache séparément comme dans un ciel étoilé. Dans ce cas, bien que chaque tache soit étendue, de taille micrométrique, il serait possible de pointer précisément la position de leur centre, et donc la position de la molécule à l’origine de cette lumière. La capacité d’allumer et d’éteindre de façon contrôlée les molécules fluorescentes permet cette localisation nanométrique. C’est ce concept révolutionnaire qui a été récompensé par un autre prix Nobel, en 2014. Ainsi, les petites molécules fluorescentes sont activées successivement, leur centre est localisé individuellement pour reconstituer toute l’image à l’échelle nanométrique.
Nanoscope
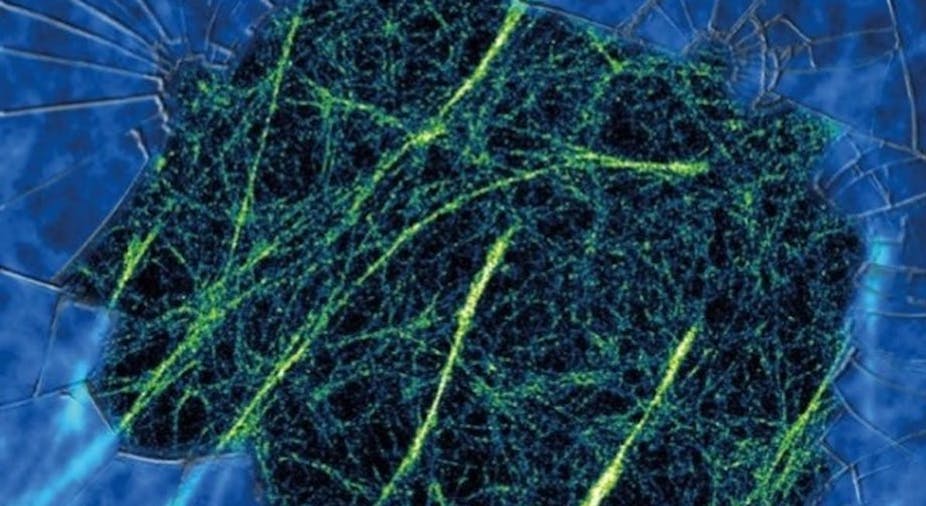
Le microscope devient alors un nanoscope. Dans les cellules, l’architecture de la vie peut se dévoiler. On observe comment le cytosquelette des cellules constitué d’un enchevêtrement de nanofilament aide les cellules à se multiplier, comment les médicaments pénètrent dans les bactéries pour les détruire, comment les cellules immunitaires ont développé des pieds nanométriques pour se mouvoir, comment les neurones élaborent des échafaudages pour construire leurs axones… L’ensemble de ces tableaux permet de mieux comprendre les mécanismes du vivant.

On pourrait penser que ces prouesses restent à ce jour confinées à la recherche fondamentale dans des laboratoires de biologie. Il n’en est rien, la nanoscopie a déjà trouvé des applications pouvant permettre de nouveaux diagnostics médicaux et en particulier des diagnostics individualisés au niveau du patient. L’Université de Wurtzbourg en Allemagne vient ainsi de lancer un centre d’immunothérapie personnalisée où l’observation à l’échelle nanoscopique des récepteurs des cellules cancéreuses permet d’évaluer le traitement le plus adéquat, augmentant ainsi l’efficacité et réduisant les effets indésirables. La nanoscopie pourrait bien devenir la clef du diagnostic médical adapté à chaque patient.

Créé en 2007, Axa Research Fund soutient plus de 500 projets à travers le monde portés par des chercheurs de 51 nationalités. Pour en savoir plus sur le travail d’Emmanuel Fort, rendez-vous sur le site du Axa Research Fund.