La pandémie de Covid-19 continue de faire des victimes partout dans le monde et les premiers candidats vaccins ne devraient pas être disponibles avant 2021 au plus tôt.
En attendant, les recherches sur les traitements continuent de mobiliser les scientifiques.
Dans cette dynamique, notre équipe vient de publier dans la revue Cell Reports Medecine des résultats précliniques prometteurs sur l’association du remdesivir avec un médicament repositionné : le diltiazem.
Une méthode novatrice de recherche de traitements antiviraux
Dans notre laboratoire VirPath à Lyon, nous menons depuis plusieurs années une stratégie de repositionnement de médicaments déjà sur le marché pour de nouvelles indications thérapeutiques, notamment anti-infectieuses.
Un terme technique pour une réalité simple : un médicament est autorisé à être mis sur le marché pour une indication médicale donnée, l’idée est de le tester, et le cas échéant de le repositionner, pour le traitement d’autres pathologies.
Vous connaissez sans doute l’histoire de la fameuse pilule bleue. A l’origine, le viagra n’était pas du tout destiné à son usage actuel. Pfizer destinait en fait la molécule (Le citrate de sildénafil, connu pour sa capacité à dilater les vaisseaux sanguins) au traitement de l’angine de poitrine. Lors des essais cliniques, la molécule s’est révélée insuffisamment efficace pour soigner cette pathologie et il a été observé des effets secondaires inattendus et pour le moins surprenants. C’est donc à partir d’une observation fortuite au cours de son développement clinique que la molécule a ainsi été repositionnée pour une nouvelle indication thérapeutique.
Pour ne pas être dépendant de la découverte fortuite d’effets imprévisibles, nous avons développé et validé au laboratoire une stratégie scientifique rationnelle et rationalisée de criblage in silico de médicaments. Cette stratégie est basée sur la caractérisation par séquençage à haut débit et sur l’analyse via des outils d’intelligence artificielle de signatures chémogénomiques et virogénomiques, qui constituent en quelque sorte les empreintes cellulaires que laissent les médicaments et les pathogènes, respectivement.
Une fois sélectionnés, les candidats à haut potentiel pour un repositionnement sont évalués pour leur propriété anti-infectieuse supposée dans différents modèles précliniques d’infection in vitro (lignées cellulaires, épithélium respiratoire humain reconstitué et cultivé en interface air/liquide) et in vivo (animaux). Le repositionnement de médicament présente des avantages majeurs par rapport au développement classique de molécule de novo, notamment celui de réduire considérablement la durée et les coûts de développement jusqu’à l’autorisation de mise sur le marché pour la nouvelle indication sur le marché, mais aussi de pouvoir répondre de manière très réactive, en allant puiser dans la pharmacopée existante, lorsque nous sommes face à l’émergence d’un nouveau pathogène contre lequel il n’existe aucun traitement ni vaccin.
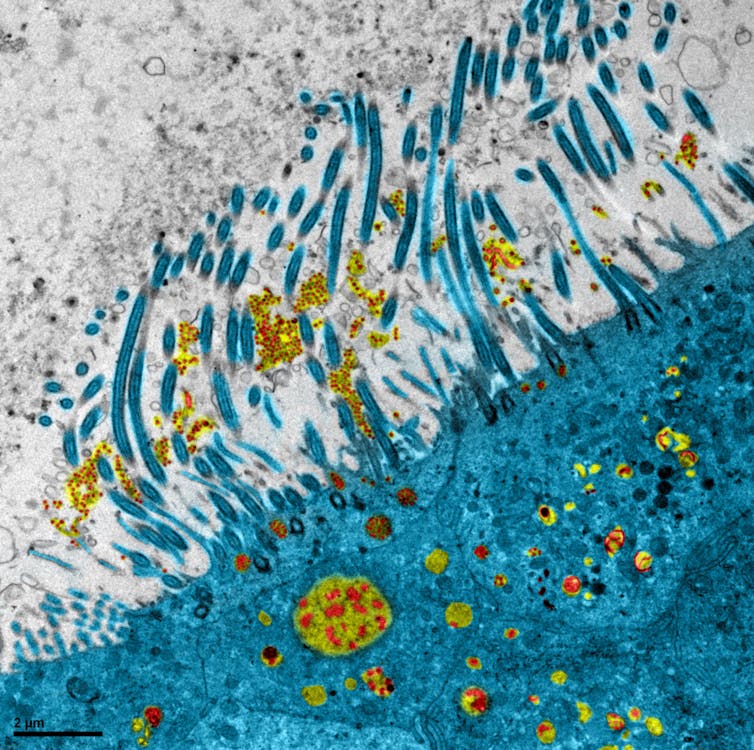
Le remdesivir est un exemple de médicament repositionné : une molécule initialement en développement pour lutter contre le virus Ebola, et pour lequel il a été montré une activité antivirale contre le SARS-CoV-2 (virus du Covid-19) dans plusieurs modèles précliniques et un potentiel à accélérer le temps de guérison chez les patients hospitalisés. Les résultats cliniques, encore incomplets, supportent l’usage du remdesivir pour soigner le Covid-19, mais, seul il n’est pas efficace pour diminuer le taux de mortalité chez les patients souffrant de forme sévère de la pathologie.
Un nouveau paradigme : la « polypharmacologie »
Jusqu’à récemment, le paradigme majeur en pharmacologie était de se dire qu’une molécule est associée spécifiquement à une cible thérapeutique donnée. Notre stratégie de repositionnement est quant à elle basée sur un nouveau paradigme, celui de la « polypharmacologie » : une molécule chimique aurait ainsi entre 6 et 13 cibles cellulaires différentes ; c’est ce qu’on appelle les effets « off target » des médicaments qui se traduisent par des effets secondaires.
Notre approche de repositionnement de médicaments pour de nouvelles indications thérapeutiques antivirales s’appuie de ce fait sur le ciblage des cellules de l’hôte, dont les virus sont entièrement dépendants pour leur réplication, plutôt que des déterminants viraux, qui mutent constamment lorsqu’il s’agit notamment de virus à ARN et en particulier respiratoires comme les virus de la grippe ou les coronavirus.
Cette stratégie peut permettre non seulement de diminuer les risques d’apparition de résistance virale, mais également d’obtenir des effets antiviraux à large spectre. Un de nos objectifs est aussi de pouvoir combiner ces médicaments repositionnés qui ciblent les cellules épithéliales respiratoires (les usines à virus), avec des antiviraux classiques pour en potentialiser l’effet. Une première preuve de concept a été faite sur les virus influenza avec l’identification et le repositionnement du diltiazem, un médicament sur le marché pour ses propriétés anti-hypertensive, comme inhibiteur des virus de la grippe dans plusieurs modèles précliniques.
Notre approche technologique nous a également permis d’identifier son mode d’action jusqu’alors inconnu, celui de stimuler la réponse immunitaire innée des muqueuses. Un essai clinique de phase 2 randomisé en double aveugle est mené depuis 3 hivers et vise à évaluer la combinaison Diltiazem + oseltamivir (Tamiflu) dans la prise en charge des patients souffrant de grippe sévère en réanimation.
Des résultats prometteurs contre le SARS-CoV-2
Dans le cadre du consortium national REACTing coordonné par l’Inserm, notre équipe a isolé dès février plusieurs souches cliniques du virus SARS-CoV-2 et développé des protocoles de quantification virale par biologie moléculaire et titrage infectieux en culture cellulaire.
Pour tester l’efficacité thérapeutique de molécules candidates contre le SARS-CoV-2, nous avons également mis en œuvre et caractérisé des modèles d’infections in vitro, et notamment basés sur des épithéliums respiratoires humains reconstitués d’origine nasale, bronchique et alvéolaire. Composés de différentes cellules primaires épithéliales (ciliée, sécrétrice de mucus, cellule de Clara, basale), organisées en tissus, ces modèles sont très physiologiques et prédictifs, tels que décrits dans l’étude récemment publiée dans la revue Nature sur l’inefficacité de l’hydroxychloroquine en modèle de primate non humain.
Nous avons évalué un grand nombre de molécules candidates dans ces modèles, dont deux molécules d’intérêt : le remdesivir et le diltiazem, en monothérapie et en combinaison. Les résultats de cette étude montrent une réduction significative de la charge virale dans les épithéliums infectés par le SARS-CoV-2 lorsqu’ils sont traités par le remdesivir. Cet effet est accru lorsque le diltiazem est ajouté en combinaison.
En stimulant la réponse immunitaire innée des épithéliums, le diltiazem potentialise ainsi l’effet du remdesivir et offre l’opportunité d’en réduire les doses chez l’homme. Cette molécule présente en effet une certaine toxicité in vivo en plus d’être un médicament très coûteux.
Vers un essai clinique
Notre équipe poursuit ses essais précliniques avec cette bithérapie dans des modèles animaux et nous espérons pouvoir lancer un essai clinique dès l’hiver prochain si les résultats positifs se confirment.
D’autres combinaisons de médicaments repositionnés sont également à l’étude.

